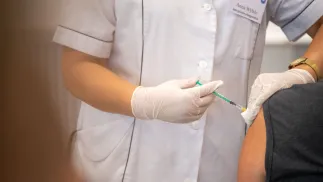
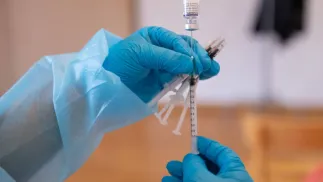
Rzecznik MZ: Polska zgłosiła zapotrzebowanie na 4 mln dawek szczepionki Nuvaxovid
Polska uczestniczy w zamówieniu unijnym na 100 mln szczepionek firmy Novavax. Mówimy w tej chwili o zgłoszonym zapotrzebowaniu na ponad 4 mln dawek, pierwsze szczepionki tej firmy powinny trafić do Polski na początku przyszłego roku - mówił rzecznik MZ Wojciech Andrusiewicz.

W poniedziałek przewodnicząca Komisji Europejskiej Ursula von der Leyen poinformowała, że KE dopuściła do obrotu w UE szczepionkę Novavax. Jest to piąta szczepionka zalecana w UE do zapobiegania Covid-19.
Andrusiewicz powiedział na konferencji prasowej, że Polska uczestniczy "w zamówieniu, w przetargu unijnym na 100 mln szczepionek firmy Novavax". "Ten przetarg jest podzielony, można powiedzieć, na dwie transze. Jedna to jest transza początkowa, a druga transza początkowa, ale z możliwością płynnej reakcji na zamówienia" - powiedział rzecznik MZ.
Wyjaśnił, że "w ramach pierwszej transzy mamy zamówionych 1 mln 800 tys. dawek, a w ramach tej drugiej elastycznej transzy mamy zamówionych 2,5 mln dawek". "Oczywiście te dawki możemy zwiększać. Więc sumarycznie mówimy w tej chwili o zgłoszonym zapotrzebowaniu z Polski, o podpisanej umowie na ponad 4 mln dawek szczepionek" - powiedział Andrusiewicz.
Nuvaxovid będzie produkowana w Polsce
Dodał, że powinny się one pojawiać od początku przyszłego roku. "Pamiętajmy też, że w Polsce będzie między innymi część produkcji się odbywała. Więc ten dostęp do szczepionek będzie bieżący" - podkreślił rzecznik resortu zdrowia.
Europejska Agencja Leków (EMA) zaleciła w poniedziałek przyznanie warunkowego pozwolenia na dopuszczenie do obrotu szczepionki Novavax Covid-19 o nazwie Nuvaxovid w celu zapobiegania infekcji koronawirusem u osób w wieku od 18 lat.
Nuvaxovid to piąta szczepionka zalecana w UE do zapobiegania Covid-19. Jest to preparat białkowy i wraz z już zatwierdzonymi szczepionkami będzie wspierać kampanie szczepień w państwach członkowskich UE w kluczowej fazie pandemii - poinformowała EMA.
Szczepionka spełnia unijne kryteria skuteczności
Po dokładnej ocenie EMA stwierdziła, że dane dotyczące szczepionki są rzetelne i spełniają unijne kryteria skuteczności, bezpieczeństwa i jakości.
Wyniki dwóch głównych badań klinicznych wykazały, że Nuvaxovid był skuteczny w zapobieganiu Covid-19 u osób w wieku 18 lat. W badaniach wzięło udział łącznie ponad 45 tys. osób. W pierwszym badaniu około dwie trzecie uczestników otrzymało szczepionkę, a pozostali otrzymali zastrzyk placebo; w drugim badaniu uczestnicy byli równo podzieleni między Nuvaxovid i placebo. Ludzie nie wiedzieli, czy otrzymali Nuvaxovid, czy placebo.
90,4 procent skuteczności nowej szczepionki
Pierwsze badanie, przeprowadzone w Meksyku i USA, wykazało 90,4 proc. skuteczności szczepionki. Drugie badanie, przeprowadzone w Wielkiej Brytanii, również wykazało podobne zmniejszenie liczby objawowych przypadków Covid-19 u osób, które otrzymały Nuvaxovid (10 przypadków z 7020 osób) w porównaniu z osobami, którym podawano placebo (96 z 7019 osób); w tym badaniu skuteczność szczepionki wyniosła 89,7 proc.
"Podsumowując, wyniki obu badań wskazują, że skuteczność szczepionki dla Nuvaxovidu wynosi około 90 proc. Pierwotny szczep SARS-CoV-2 i niektóre warianty wzbudzające obawy, takie jak Alfa i Beta, były najczęstszymi szczepami wirusowymi krążącymi w trakcie badań. Obecnie dostępne są ograniczone dane dotyczące skuteczności leku Nuvaxovid wobec innych budzących obawy wariantów, w tym Omikron" - oświadczyła EMA.
Działania niepożądane
Działania niepożądane obserwowane podczas stosowania Nuvaxovidu w badaniach były zwykle łagodne lub umiarkowane i ustępowały w ciągu kilku dni po szczepieniu. Najczęstsze z nich to ból w miejscu wstrzyknięcia, zmęczenie, ból mięśni, ból głowy, ogólne złe samopoczucie, ból stawów oraz nudności lub wymioty.
Bezpieczeństwo i skuteczność szczepionki będą nadal monitorowane w miarę jej stosowania w całej UE za pośrednictwem unijnego systemu nadzoru nad bezpieczeństwem farmakoterapii oraz dodatkowych badań prowadzonych przez firmę i władze europejskie - podała EMA. (PAP)
Autor: Edyta Roś
ja/